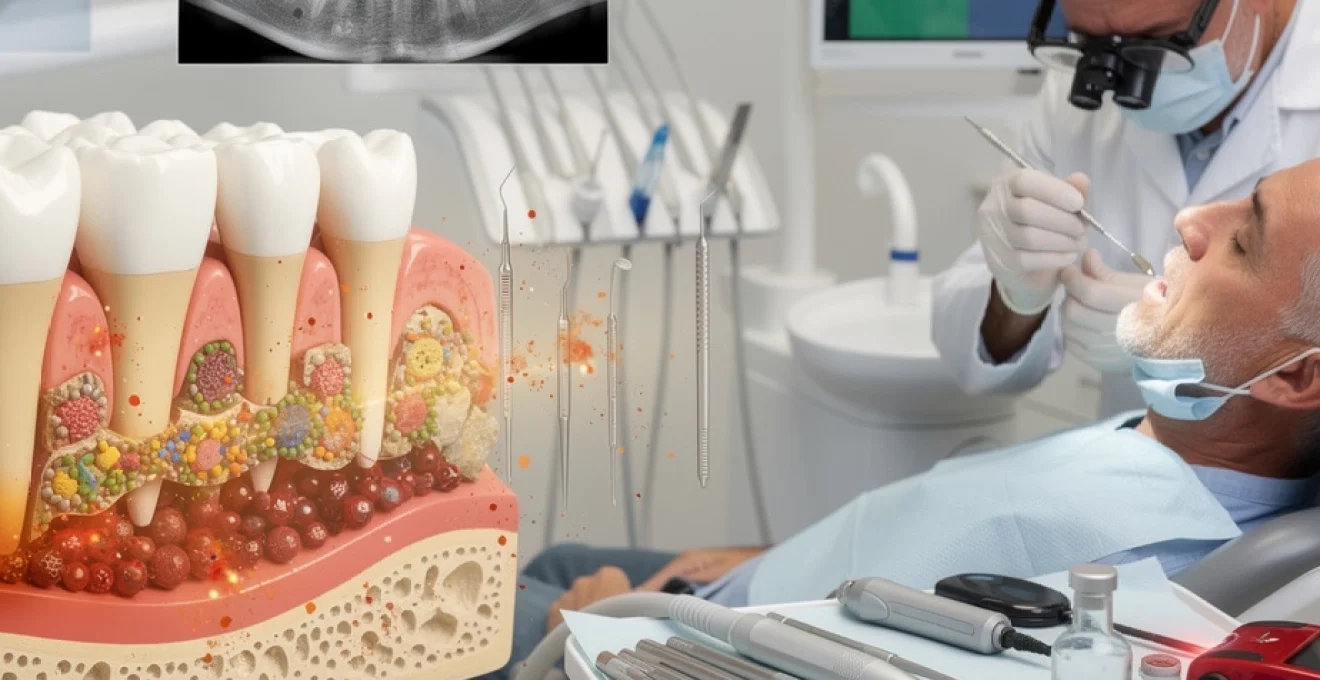
La parodontite représente l’une des pathologies bucco-dentaires les plus répandues au monde, touchant près de 30 % des adultes français selon les dernières études épidémiologiques. Cette maladie infectieuse chronique, caractérisée par la destruction progressive des tissus de soutien dentaire, constitue la principale cause de perte dentaire chez l’adulte après 35 ans. Contrairement à une gingivite superficielle, la parodontite atteint les structures profondes du parodonte, engendrant des conséquences irréversibles sur l’os alvéolaire et le ligament parodontal. Sa nature silencieuse et évolutive en fait un enjeu majeur de santé publique, d’autant plus que les recherches récentes établissent des corrélations significatives entre cette pathologie et diverses maladies systémiques telles que le diabète et les affections cardiovasculaires.
Étiopathogénie de la parodontite : mécanismes inflammatoires et facteurs de risque
Biofilm bactérien et complexes microbiens de socransky dans la genèse parodontale
La formation du biofilm bactérien constitue l’élément déclencheur de la cascade pathologique parodontale. Cette pellicule microbienne organisée adhère fermement aux surfaces dentaires grâce à une matrice extracellulaire composée de polysaccharides, de protéines et d’ADN bactérien. Les complexes microbiens de Socransky, particulièrement le complexe rouge comprenant Porphyromonas gingivalis, Treponema denticola et Tannerella forsythia, jouent un rôle prépondérant dans l’initiation des lésions parodontales. Ces bactéries anaérobies à Gram négatif sécrètent de puissantes endotoxines et des facteurs de virulence qui perturbent l’équilibre de l’écosystème buccal.
L’établissement de ce biofilm pathogène s’effectue selon une succession temporelle précise. Initialement, les bactéries pionnières comme Streptococcus sanguis colonisent la surface dentaire, créant un environnement propice à l’adhésion de micro-organismes plus pathogènes. Cette colonisation secondaire implique des interactions complexes de coagrégation et de communication intercellulaire, aboutissant à la formation d’une communauté microbienne mature résistante aux mécanismes de défense de l’hôte.
Cascade inflammatoire et libération de cytokines pro-inflammatoires IL-1β et TNF-α
La réponse immuno-inflammatoire de l’hôte face à l’agression bactérienne déclenche une cascade inflammatoire complexe orchestrée par de nombreux médiateurs. L’interleukine-1β (IL-1β) et le facteur de nécrose tumorale alpha (TNF-α) constituent les cytokines pro-inflammatoires majeures impliquées dans la destruction tissulaire parodontale. Ces molécules activent les ostéoclastes responsables de la résorption osseuse et stimulent la production de métalloprotéinases matricielles (MMP) qui dégradent le collagène du ligament parodontal.
L’activation des cellules dendritiques et des macrophages gingivaux amplifie cette réponse inflammatoire par la sécrétion d’autres médiateurs comme l’IL-6, l’IL-8 et la prostaglandine E2. Cette hyperactivation du système immunitaire, initialement protectrice, devient délétère lorsqu’elle persiste
et s’auto-entretient, même en l’absence de stimulation bactérienne massive. C’est précisément ce déséquilibre entre agression microbienne et défense de l’hôte qui transforme une simple gingivite réversible en véritable parodontite destructive. Vous l’aurez compris : dans la parodontite, ce n’est pas seulement la présence de bactéries qui pose problème, mais surtout la manière dont votre organisme y répond sur le long terme.
Facteurs de risque systémiques : diabète de type 2 et polymorphismes génétiques IL-1
Au-delà du biofilm, certains facteurs systémiques modulent fortement la susceptibilité à la parodontite. Le diabète de type 2 est aujourd’hui reconnu comme l’un des principaux facteurs de risque de maladie parodontale. Une hyperglycémie chronique favorise la formation de produits de glycation avancée (AGEs) qui se lient à leurs récepteurs (RAGE) sur les cellules immunitaires, amplifiant la production de cytokines pro-inflammatoires et de radicaux libres. Résultat : les tissus de soutien de la dent sont plus vulnérables et la cicatrisation est nettement ralentie.
Sur le plan génétique, plusieurs études ont mis en évidence l’implication de polymorphismes des gènes codant pour l’interleukine-1 (complexe IL-1). Certains profils génétiques seraient associés à une réponse inflammatoire exacerbée, avec une production accrue d’IL‑1β en présence de plaque dentaire. Ces individus présentent un risque plus élevé de développer une parodontite sévère, plus tôt dans la vie, même avec une hygiène bucco-dentaire apparemment correcte. Bien entendu, ces polymorphismes ne « condamnent » pas à la parodontite, mais ils augmentent la nécessité d’un suivi parodontal régulier.
Diabète mal équilibré et susceptibilité génétique ne sont pas des fatalités : ils rappellent simplement que la parodontite est une maladie multifactorielle. En travaillant sur votre équilibre glycémique, vos habitudes de vie et une hygiène bucco-dentaire rigoureuse, vous pouvez compenser en partie cette vulnérabilité. D’où l’importance d’une approche personnalisée : deux patients présentant la même quantité de plaque ne développeront pas forcément la même sévérité de parodontite.
Impact du tabagisme sur la microcirculation gingivale et la cicatrisation parodontale
Le tabagisme constitue l’un des facteurs aggravants les plus documentés en parodontologie. La nicotine et les autres composants toxiques de la fumée altèrent la microcirculation gingivale en provoquant une vasoconstriction et une diminution de l’apport sanguin. Paradoxalement, les gencives des fumeurs saignent souvent moins, non pas parce qu’elles sont saines, mais parce que leur vascularisation est compromise. C’est un peu comme si l’alarme incendie était coupée alors que le feu continue de se propager en coulisses.
Sur le plan cellulaire, le tabac perturbe la fonction des neutrophiles, des fibroblastes et des ostéoblastes, ce qui compromet la défense vis-à-vis des bactéries et la capacité de cicatrisation des tissus parodontaux. Les fumeurs présentent ainsi plus de poches parodontales profondes, une perte osseuse plus marquée et une réponse moins prévisible aux traitements, qu’ils soient non chirurgicaux ou chirurgicaux. La régénération osseuse guidée ou les greffes de gencive affichent également des taux de succès inférieurs chez les gros fumeurs.
Faut-il pour autant renoncer à traiter la parodontite chez un patient fumeur ? Bien au contraire. Les études montrent qu’un sevrage tabagique, même partiel, améliore significativement la réponse au traitement parodontal. Si vous fumez, votre chirurgien-dentiste ou votre hygiéniste bucco-dentaire pourra vous proposer un accompagnement ou vous orienter vers des programmes de sevrage adaptés. C’est un investissement doublement rentable : pour vos gencives, mais aussi pour votre santé générale.
Classifications cliniques et diagnostic différentiel des maladies parodontales
Classification AAP/EFP 2017 : parodontite par stades et grades de sévérité
La compréhension moderne de la parodontite s’appuie sur la classification AAP/EFP de 2017, qui remplace les anciennes terminologies parfois déroutantes pour les patients. Ce système classe la parodontite selon des stades (I à IV) basés sur la sévérité et la complexité du cas, et des grades (A à C) reflétant la vitesse de progression et les facteurs de risque. Concrètement, cela permet de passer d’une simple étiquette de « parodontite chronique » à une véritable carte d’identité de la maladie.
Les stades reposent principalement sur la perte d’attache clinique, la perte osseuse radiographique et le nombre de dents perdues pour raison parodontale. Le stade I correspond à une atteinte initiale, tandis que le stade IV décrit des destructions sévères compromettant la fonction masticatoire. Les grades, eux, intègrent la vitesse de progression, le tabagisme, le diabète et la réponse au traitement. Un patient peut ainsi être classé « parodontite stade III, grade C », indiquant une forme avancée à progression rapide nécessitant un contrôle très rigoureux.
Pourquoi cette classification est-elle importante pour vous ? Parce qu’elle permet un plan de traitement personnalisé et un meilleur suivi dans le temps. Votre praticien peut vous expliquer clairement le niveau de sévérité, les risques d’évolution et les objectifs de stabilisation. C’est un peu comme passer d’une simple indication « hypertension » à une description précise de votre tension, de vos facteurs de risque et de votre cible thérapeutique.
Indice de saignement papillaire de mühlemann et mesures de profondeur de sondage
Sur le plan clinique, le diagnostic de parodontite repose sur un examen systématique des gencives. L’un des outils les plus utilisés est l’indice de saignement papillaire de Mühlemann, qui évalue la tendance au saignement des papilles interdentaires après une légère stimulation à la sonde. Un pourcentage élevé de sites saignants signale une inflammation active, souvent corrélée à un risque accru de progression parodontale. Pour vous, cela se traduit par cette question centrale : « Mes gencives saignent-elles au brossage ou à la moindre sollicitation ? »
La mesure de la profondeur de sondage à l’aide d’une sonde millimétrée permet de quantifier les poches parodontales. Des valeurs supérieures à 4 mm, surtout si elles s’accompagnent de saignement et de perte d’attache, signent la présence de poches pathologiques. Le praticien enregistre ces données dent par dent, souvent sous forme de parodontal charting, pour suivre l’évolution avant et après traitement. Cet examen est généralement indolore, même s’il peut être légèrement inconfortable en cas d’inflammation importante.
En combinant l’indice de saignement et les profondeurs de sondage, l’équipe soignante peut cibler les zones prioritaires de traitement et évaluer l’efficacité de vos efforts d’hygiène bucco-dentaire. Lors des séances de maintenance, la diminution du saignement et la réduction des poches constituent des indicateurs très concrets de stabilisation de votre parodontite. Vous devenez ainsi acteur de votre traitement, en visualisant les progrès obtenus.
Radiographie rétroalvéolaire et analyse de la perte osseuse horizontale versus verticale
L’examen clinique est toujours complété par une évaluation radiographique pour apprécier la perte osseuse alvéolaire. Les radiographies rétroalvéolaires, réalisées dent par dent, offrent une vision détaillée des septa osseux interdentaires et de la topographie de la destruction. On distingue classiquement une perte osseuse horizontale, où le niveau osseux reste parallèle à la jonction amélo-cémentaire, et une perte osseuse verticale, avec des défauts angulaires plus profonds sur certains sites.
Pourquoi cette distinction est-elle importante ? Les défauts osseux verticaux, en forme de cratère, sont souvent plus favorables aux techniques de régénération tissulaire guidée, car ils constituent une sorte de « contenant » naturel pour les biomatériaux. À l’inverse, les pertes horizontales diffuses se prêtent davantage à un traitement non chirurgical intensif et à une chirurgie de résection ou de réaménagement gingival lorsque nécessaire. La radiographie panoramique peut compléter l’examen, mais elle reste moins précise pour l’analyse fine de chaque site.
Dans certains cas complexes, votre praticien pourra recourir à un cone beam (CBCT), une imagerie 3D qui offre une visualisation volumique de l’os alvéolaire et des structures anatomiques voisines. Cette technologie est particulièrement utile pour planifier des chirurgies régénératrices ou des implants dans un contexte de parodontite stabilisée. Là encore, l’objectif reste le même : documenter précisément la situation de départ pour choisir la stratégie thérapeutique la plus adaptée.
Diagnostic différentiel avec la gingivite ulcéro-nécrotique aiguë de vincent
Toutes les inflammations gingivales ne sont pas synonymes de parodontite. La gingivite ulcéro-nécrotique aiguë de Vincent (GUNA) en est un bon exemple. Cette affection aiguë, souvent liée au stress, au tabagisme important et à une hygiène déficiente, se manifeste par des douleurs intenses, une halitose fétide et des ulcérations nécrotiques des papilles interdentaires. Contrairement à la parodontite chronique, la GUNA évolue rapidement mais reste essentiellement superficielle si elle est traitée à temps.
Le diagnostic différentiel repose sur la chronologie, la symptomatologie et les examens cliniques. Dans la parodontite, la douleur est souvent absente ou modérée, l’évolution est lente et les poches parodontales profondes avec perte d’attache sont au premier plan. Dans la GUNA, la douleur est aiguë, les ulcérations sont caractéristiques et la destruction tissulaire profonde n’est pas initialement présente. Un traitement rapide à base de débridement local, d’antiseptiques et parfois d’antibiotiques permet généralement une résolution complète.
Vous vous demandez peut-être : la GUNA peut-elle évoluer vers une parodontite ? Indirectement, oui, si le terrain inflammatoire et les facteurs de risque persistent, car la plaque dentaire et le biofilm se reconstituent rapidement. D’où la nécessité, une fois l’épisode aigu contrôlé, d’instaurer une prévention parodontale durable avec des conseils d’hygiène et un suivi régulier.
Protocoles thérapeutiques non-chirurgicaux : débridement et surfaçage radiculaire
Détartrage-surfaçage par quadrants avec curettes de gracey spécifiques
La pierre angulaire du traitement de la parodontite reste le détartrage-surfaçage radiculaire non chirurgical. L’objectif est simple en théorie : éliminer le tartre et le biofilm sous-gingival, lisser les surfaces radiculaires pour réduire l’adhésion bactérienne et permettre la réadaptation de la gencive à la dent. En pratique, ce travail minutieux se fait généralement par quadrants (hémi-arcades) au cours de plusieurs séances, afin de garantir un nettoyage en profondeur tout en préservant votre confort.
Les curettes de Gracey, instruments manuels spécialement conçus pour les différentes faces radiculaires, restent une référence en parodontologie. Associées aux inserts ultrasoniques fins, elles permettent de travailler dans les poches étroites et profondes, parfois jusqu’à 6 ou 7 mm, sans traumatiser excessivement les tissus. Une anesthésie locale peut être proposée pour les zones les plus sensibles, mais de nombreux patients tolèrent très bien le traitement avec une simple anesthésie de contact.
Après un débridement complet, il est fréquent de constater une diminution des saignements, une réduction des poches et parfois une légère sensibilité dentaire transitoire liée à l’exposition des collets. C’est le signe que l’inflammation recule et que la gencive se resserre autour des dents. Vous aurez alors un rôle clé : maintenir une hygiène bucco-dentaire quotidienne irréprochable pour empêcher une recolonisation rapide des poches par des bactéries pathogènes.
Thérapie photodynamique au bleu de méthylène et laser diode 670nm
Pour renforcer l’action mécanique du débridement, certaines équipes proposent une thérapie photodynamique comme adjuvant. Le principe ? Un colorant photosensibilisant, souvent du bleu de méthylène, est appliqué dans les poches parodontales, où il se fixe préférentiellement sur les bactéries. Un laser diode de longueur d’onde adaptée (par exemple 670 nm) est ensuite utilisé pour activer ce colorant, générant des radicaux oxygénés capables de détruire sélectivement les micro-organismes.
Cette approche, non invasive et indolore, vise à réduire davantage la charge bactérienne, en particulier dans les poches profondes difficiles d’accès mécanique. Elle peut être intéressante chez les patients présentant des contre-indications aux antibiotiques systémiques ou dans les cas de parodontites agressives. Toutefois, la thérapie photodynamique ne remplace pas le surfaçage : elle vient en complément, comme une désinfection renforcée des zones critiques.
Les études cliniques montrent une amélioration modérée mais significative des paramètres parodontaux (profondeurs de sondage, saignement) lorsqu’elle est associée à un traitement conventionnel bien conduit. Comme pour tout traitement avancé, la sélection des cas et l’expertise de l’équipe soignante sont essentielles pour en tirer le meilleur bénéfice.
Antibiothérapie adjuvante : amoxicilline-métronidazole selon protocoles van winkelhoff
Dans certaines situations, notamment en présence de parodontite sévère généralisée ou de formes à progression rapide chez des patients jeunes, une antibiothérapie adjuvante peut être indiquée. Le protocole le plus étudié reste l’association amoxicilline + métronidazole, souvent appelée protocole de Van Winkelhoff. Administrée par voie générale, cette combinaison vise à cibler les bactéries anaérobies Gram négatif du complexe rouge et orange impliquées dans la destruction parodontale.
Le timing est capital : l’antibiothérapie est généralement initiée au moment ou juste après le débridement complet, afin de limiter la recolonisation des poches en phase de cicatrisation. La durée de traitement est courte (environ une semaine), ce qui réduit le risque d’effets secondaires et de résistance bactérienne, à condition que l’indication soit bien posée. Il ne s’agit donc pas d’un traitement « automatique », mais d’un outil supplémentaire dans les cas sélectionnés.
Avant de prescrire des antibiotiques, votre praticien vérifiera les contre-indications potentielles (allergies, grossesse, interactions médicamenteuses, troubles hépatiques ou rénaux). Il vous rappellera également l’importance de respecter scrupuleusement la posologie et la durée du traitement. Sans hygiène bucco-dentaire rigoureuse et sans surfaçage soigné, l’antibiothérapie seule n’a aucun intérêt en parodontite.
Maintenance parodontale et contrôle de plaque selon l’indice de silness et löe
Une fois la phase active de traitement terminée, tout commence vraiment : c’est la phase de maintenance parodontale. L’enjeu est clair : éviter la rechute et maintenir les résultats obtenus sur le long terme. Pour cela, votre praticien s’appuie souvent sur l’indice de plaque de Silness et Löe, qui évalue la quantité de plaque présente le long du rebord gingival. Cet indice, simple à mesurer, permet de suivre objectivement la qualité de votre brossage et de vos gestes interdentaires.
Concrètement, lors des séances de maintenance (tous les 3, 4 ou 6 mois selon votre risque), un détartrage d’entretien est réalisé, les poches sont sondées et votre technique de brossage est réévaluée. Des ajustements peuvent être proposés : changement de brosse à dents, ajout de brossettes interdentaires, modification de la méthode de brossage. C’est un véritable travail en binôme entre vous et l’équipe soignante.
Vous vous demandez peut-être : « Pourquoi revenir si souvent si ma parodontite est stabilisée ? » Parce que le biofilm se reforme en quelques heures et que la susceptibilité inflammatoire de vos tissus ne disparaît pas. La maintenance permet de casser régulièrement le cycle inflammatoire, de détecter précocement toute réactivation et d’adapter vos soins au fil du temps. C’est le prix, raisonnable, à payer pour conserver vos dents et un sourire sain le plus longtemps possible.
Approches chirurgicales régénératrices et reconstructrices avancées
Lorsque le traitement non chirurgical ne suffit pas à réduire certaines poches profondes ou à restaurer une architecture tissulaire fonctionnelle, des approches chirurgicales parodontales peuvent être proposées. L’objectif n’est plus seulement de contrôler l’infection, mais aussi de reconstruire autant que possible les tissus perdus ou de réaménager les contours gingivaux pour faciliter l’hygiène. C’est un peu comme passer du simple débroussaillage à la rénovation complète d’un terrain.
Les techniques régénératrices, telles que la régénération tissulaire guidée (RTG), utilisent des membranes barrières résorbables ou non résorbables pour favoriser la repousse sélective de l’os et du ligament parodontal dans les défauts osseux verticaux. Elles peuvent être associées à des substituts osseux (xénogreffes, allogreffes, biomatériaux synthétiques) et à des facteurs de croissance dérivés du sang du patient (PRF, PRP) afin d’améliorer la qualité de la cicatrisation. Ces protocoles sont particulièrement indiqués autour de dents stratégiques présentant des poches isolées profondes.
Parallèlement, les chirurgies muco-gingivales et les greffes de tissu conjonctif permettent de traiter les récessions gingivales, de renforcer la gencive attachée et de corriger certaines séquelles esthétiques de la parodontite. Dans les cas les plus avancés (stade IV), des chirurgies de résection, de réaménagement des cratères osseux ou de réhabilitation globale avec implants peuvent être envisagées, une fois la maladie stabilisée. Là encore, la clé du succès reste un contrôle rigoureux de la plaque avant et après l’intervention.
Complications systémiques et interactions médicamenteuses de la parodontite
La parodontite n’est pas qu’un problème de gencives : c’est une véritable infection chronique à bas bruit qui peut influencer l’état de santé général. De nombreuses données suggèrent un lien bidirectionnel entre parodontite et diabète de type 2, la maladie parodontale compliquant l’équilibre glycémique et, inversement, l’hyperglycémie aggravant l’inflammation parodontale. De plus, la présence de bactéries parodontopathogènes et de cytokines pro-inflammatoires dans la circulation pourrait contribuer au risque cardiovasculaire, en participant à la formation ou à la déstabilisation des plaques d’athérome.
Certaines populations sont particulièrement concernées : les femmes enceintes, chez lesquelles une parodontite active est associée à un risque accru d’accouchement prématuré et de faible poids de naissance, ou encore les patients immunodéprimés. Dans tous ces cas, la prise en charge parodontale s’intègre dans une approche globale de la santé, en lien avec le médecin traitant ou les spécialistes. Avez-vous déjà envisagé que traiter vos gencives puisse aussi contribuer à réduire certains risques systémiques ?
Par ailleurs, plusieurs médicaments couramment prescrits peuvent interagir avec la santé parodontale ou avec les traitements parodontaux. Les anti-inflammatoires non stéroïdiens, les anticoagulants, certains antihypertenseurs ou antidépresseurs peuvent modifier la réponse inflammatoire, le saignement ou la cicatrisation. D’autres molécules, comme les antiépileptiques (phénytoïne) ou les inhibiteurs calciques, sont connues pour favoriser une hyperplasie gingivale, compliquant l’hygiène et augmentant le risque de parodontite.
C’est pourquoi il est essentiel d’informer votre chirurgien-dentiste de tous les médicaments que vous prenez, y compris les traitements ponctuels ou les compléments alimentaires. De son côté, l’équipe soignante adaptera les protocoles (choix des anesthésiques, antibiotiques, antalgiques) et, si nécessaire, échangera avec votre médecin pour sécuriser la prise en charge. La parodontite étant au carrefour de nombreuses disciplines, une communication fluide entre les professionnels de santé est un véritable atout.
Prévention tertiaire et protocoles de maintenance parodontale à long terme
Une fois la parodontite stabilisée, la priorité devient la prévention tertiaire, c’est-à-dire la prévention des récidives et des complications à long terme. Cela passe d’abord par l’adoption de routines d’hygiène bucco-dentaire adaptées : brossage biquotidien avec une brosse souple (manuelle ou électrique), utilisation quotidienne de brossettes interdentaires ou de fil dentaire, et recours éventuel à des bains de bouche antiseptiques en cure courte sur conseil du praticien. L’idée n’est pas de faire plus, mais de faire mieux et régulièrement.
Les protocoles de maintenance parodontale s’appuient sur une stratification du risque : plus votre parodontite était sévère, plus vos facteurs de risque (tabac, diabète, antécédents familiaux) sont présents, plus les contrôles devront être rapprochés, parfois tous les 3 mois. Lors de ces visites, le professionnel vérifie l’absence de poches actives, réalise un détartrage d’entretien, mesure les indices de plaque et de saignement, et renforce les conseils personnalisés. C’est une sorte de « révision régulière » de votre parodonte, comparable à l’entretien d’un véhicule que l’on souhaite garder longtemps en bon état.
À long terme, cette maintenance permet non seulement de préserver vos dents, mais aussi de créer un cercle vertueux pour votre santé générale. De plus en plus d’études suggèrent qu’un contrôle efficace de l’inflammation parodontale pourrait participer à une meilleure stabilité de certaines pathologies chroniques, comme le diabète ou les maladies cardiovasculaires. En prenant soin de vos gencives aujourd’hui, vous agissez donc bien au-delà de votre sourire : vous investissez dans votre capital santé global.